戈来雷塞(Glecirasib, JAB-21822)是加科思自主研发的KRAS G12C变构抑制剂,初步临床效果积极,是潜在的同类最佳分子。戈来雷塞可作为单药用于治疗带有KRAS G12C突变的非小细胞肺癌、结直肠癌等实体瘤,与SHP2i、EGFRi等联合用药,有望实现更优疗效,以及克服继发性耐药。
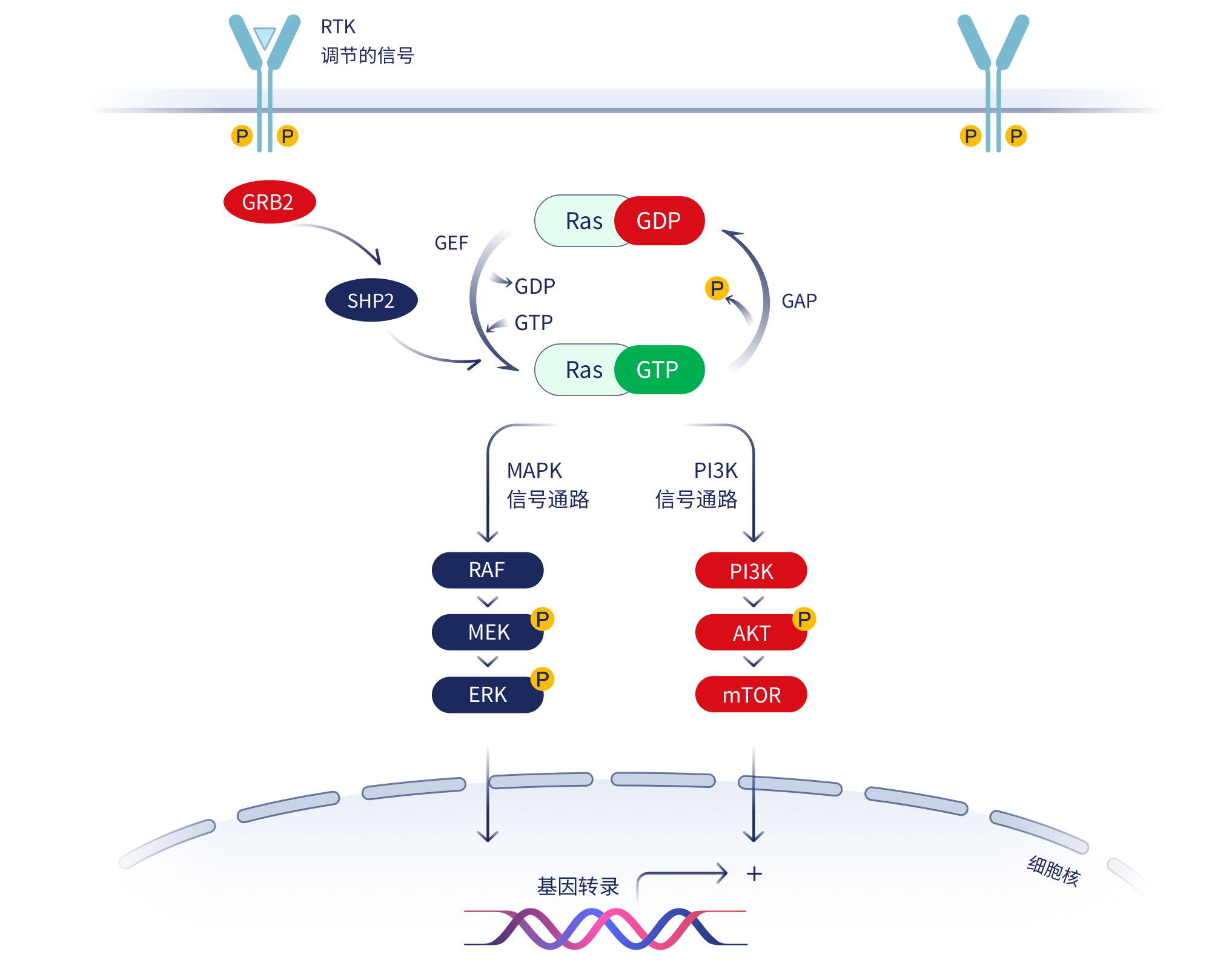
KRAS属于小GTP酶家族,是肿瘤中最常见的突变基因之一,其促肿瘤生长的生物学功能已被广泛验证。KRAS蛋白12位的甘氨酸突变为半胱氨酸(G12C),导致下游RAF-MEK-ERK等信号通路的持续激活,致使肿瘤细胞不断增殖。
尽管KRAS被发现已近40年,但由于蛋白表面光滑且缺乏小分子药物结合口袋,KRAS一直被业界视作“不可成药靶点”。直到2013年加州大学旧金山分校的Kevan M. Shokat教授发现了一个可被诱导产生的新的结合口袋(Swtich II),才为KRAS抑制剂的开发带来曙光。加科思通过自有的诱导变构新药发现平台设计了小分子变构抑制剂戈来雷塞。
戈来雷塞是一种强效的、不可逆的KRAS G12C抑制剂。戈来雷塞通过共价结合于KRAS G12C的12位突变的半胱氨酸残基上,使KRAS G12C锁定在非活化状态,从而阻断KRAS依赖的信号转导,抑制肿瘤细胞的增殖,并诱导细胞凋亡。
戈来雷塞分子不仅具有高选择性与高活性,其独特的分子结构使其具有独特的成药性,在初步的临床研究中展现出更好的药效和安全性,其极低的胃肠道毒性在临床应用中具有更好的患者依从性。戈来雷塞是潜在的同类最佳分子,有望使KRAS G12C突变的非小细胞肺癌、结直肠癌患者获益。
|
药物 |
地区 |
试验阶段 |
适应症 |
登记信息 |
|---|---|---|---|---|
|
戈来雷塞 |
中国 |
IIb期注册性临床 |
非小细胞肺癌 |
ClinicalTrials: NCT05276726 CDE Number: CTR20220492 |
|
中国 |
IIb期注册性临床 |
KRAS G12C 突变的胰腺癌、结直肠癌及其他实体瘤 |
CDE Number: CTR20211470 ClinicalTrials: NCT05009329 |
|
|
全球 |
IIa期 |
KRAS G12C 突变的非小细胞肺癌、胰腺癌、结直肠癌及其他实体瘤 |
ClinicalTrials: NCT05002270 |
|
药物 |
联合用药搭档 |
地区 |
试验阶段 |
适应症 |
登记信息 |
|---|---|---|---|---|---|
|
戈来雷塞 |
西妥昔单抗 (EGFR mAb) |
中国 |
IIa期 |
晚期结直肠癌等 |
ClinicalTrilas: NCT05194995 CDE Number: CTR20220015 |
|
帕博利珠单抗 (PD-1 mAb) |
中国 |
I期 |
晚期非小细胞肺癌 |
尚未登记 |
|
|
JAB-3312 (SHP2i) |
中国 |
IIa期 |
晚期实体瘤 |
ClinicalTrials: NCT05288205 CDE Number: CTR20220587 |
加科思在2022年欧洲肿瘤内科学会亚洲会议(ESMO ASIA)公布戈来雷塞与JAB-3312联合用药的临床前研究成果